Les maladies génétiques du développement vs les maladies génétiques dégénératives
 Les maladies génétiques peuvent également être classées en fonction du moment où elles affectent l’animal. Les maladies génétiques du développement apparaissent souvent peu après la naissance ou chez le jeune chiot. Les maladies génétiques dégénératives affectent l’animal adulte, qu’il soit plus jeune ou plus âgé.
Les maladies génétiques peuvent également être classées en fonction du moment où elles affectent l’animal. Les maladies génétiques du développement apparaissent souvent peu après la naissance ou chez le jeune chiot. Les maladies génétiques dégénératives affectent l’animal adulte, qu’il soit plus jeune ou plus âgé.
Les maladies génétiques qui sont apparentes avant que l’animal ne soit en âge de procréer sont plus faciles à contrôler et à éliminer d’une race parce que les animaux affectés ne seront pas utilisés pour la reproduction. Les maladies génétiques qui affectent les animaux plus tard dans la vie, après les années de reproduction, sont beaucoup plus difficiles à contrôler et à éliminer. La génétique nocive a souvent déjà été transmise à la génération suivante avant que la maladie ne devienne apparente.
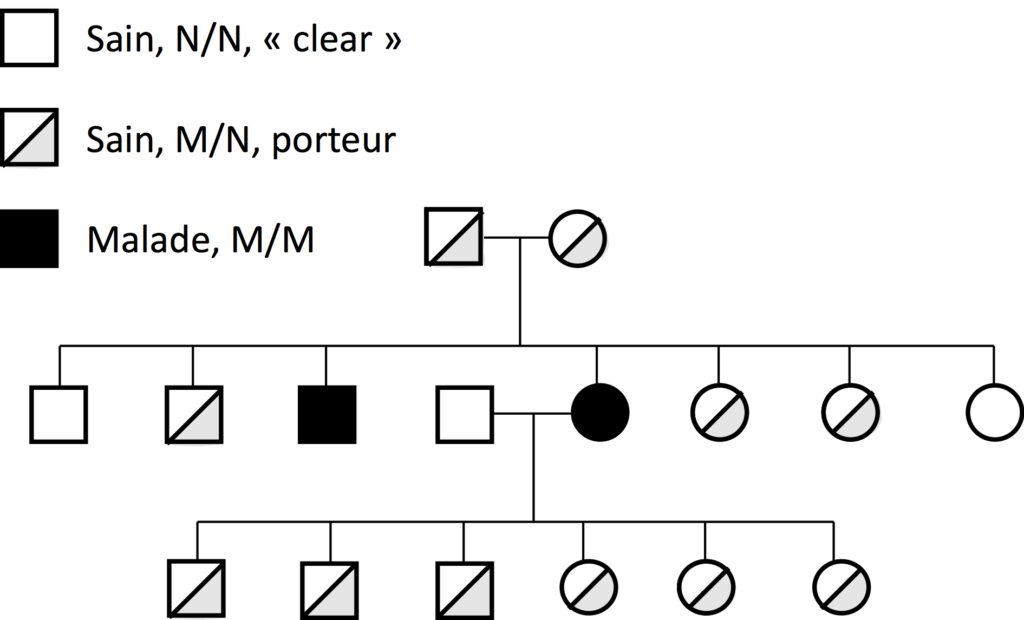
Les maladies génétiques peuvent provoquer chez le chien des symptômes pouvant être légers et contrôlables avec un traitement médical ou alors, sévères et même potentiellement mortels. Les animaux porteurs silencieux (M/N) de maladies génétiques récessives sont historiquement problématiques en raison de la difficulté à les identifier. Ils mènent une vie normale et en bonne santé, mais lorsqu’ils sont utilisés pour la reproduction, ils peuvent transmettre une copie de M à la génération suivante.
La fréquence des maladies génétiques simples chez les chiens
 Il est vrai que les maladies génétiques simples se retrouvent à une fréquence plus élevée dans nos populations de chiens domestiques que chez l’Homme, en particulier chez les chiens de race pure.
Il est vrai que les maladies génétiques simples se retrouvent à une fréquence plus élevée dans nos populations de chiens domestiques que chez l’Homme, en particulier chez les chiens de race pure.
Un exemple de maladie génétique simple chez l’Homme est la fibrose kystique. Il s’agit d’une maladie autosomique récessive avec une fréquence d’environ 1 personne affectée (M/M) sur 3 000 personnes et une fréquence de porteurs (M/N) d’environ 1 personne sur 25. Pour ce qui est des maladies génétiques simples dans les races de chien, il n’est pas rare d’avoir 1 animal affecté (ou plus) sur 100 et une fréquence d’environ 1 animal (ou plus) sur 10 qui est porteur.
La raison pour cette différence de fréquence des maladies génétiques réside dans les génomes simplifiés observés chez le chien en raison du degré de consanguinité rencontré chez les races de chiens. La consanguinité est introduite à plusieurs niveaux :
- La création de chiens de race pure au cours des 100 à 150 dernières années avec une définition des normes d’une race et une sélection intensive à partir d’un stock de fondation limité. Il s’agit, par définition, de la consanguinité.
- Livres généalogiques fermés, dans lesquels les parents doivent être enregistrés avant que la progéniture ne puisse l’être. La race devient une boîte génétique fermée qui exacerbe la consanguinité.
- La compétition moderne de chiens représente une arène de sélection artificielle dans laquelle les chiens gagnants deviendront les parents de la prochaine génération d’animaux. Avec la sélection artificielle, ce sont les gens (nous) qui décident quels animaux vont transmettre leur génétique (bonne ou mauvaise) à la génération suivante.
- Les inégalités entre la reproduction masculine et féminine permettent au chien mâle gagnant de répandre sa génétique (bonne et mauvaise). Ce phénomène est connu sous le nom de « popular sire effect ».
Les mutations génétiques
La nature des mutations mérite quelques mots d’explication. Une mutation génétique implique une modification d’une séquence d’ADN. Les mutations représentent les variations naturelles de notre ADN dont nous avons besoin pour survivre, pour nous adapter et pour évoluer en tant qu’espèce. Les mutations associées à la reproduction naturelle permettent une sélection naturelle via la « survie du plus apte ».
Une mutation de substitution est une mutation impliquant le remplacement simple d’une lettre par une autre provenant des 3 milliards retrouvées dans le texte d’ADN qui constitue notre génome (ou celui d’un chien). Une mutation d’insertion (ou de délétion) correspond à l’addition (ou à l’élimination d’une ou de plusieurs lettres dans notre texte d’ADN. Dans chaque cas, qu’il s’agisse d’une mutation par substitution, insertion ou délétion, le texte de l’ADN est modifié et ne raconte plus tout à fait la même histoire.
Le changement peut être bon, mauvais ou indifférent (neutre) pour l’animal. Les mauvaises mutations sont nombreuses et pourraient avoir des retombées désastreuses, à l’exception du fait que Dame Nature a conservé un « as » génétique en nous donnant deux copies de chacun de nos gènes. Oui, nous avons deux parents pour une raison, veuillez-vous référer à la section Génétique du chien 1,0 : Concepts de base, et n’oubliez pas de remercier vos parents. Actuellement, les avantages potentiels des quelques bonnes mutations l’emportent sur les inconvénients potentiels des plusieurs mauvaises mutations. Les variations génétiques sont bonnes, tant et aussi longtemps que nous avons la sélection naturelle. Le problème est que, chez les animaux domestiques, nous n’en avons plus.

Plusieurs exemples
Nous pouvons à présent examiner quelques exemples réels de maladies génétiques observées chez le chien. Pour une liste complète des maladies génétiques simples du chien avec des descriptions et des références, veuillez-vous référer à https://labgenvet.ca/recherche-de-maladies-genetiques-canines/.
PRA de Type 1 (Épagneuls nains continentaux / Papillons)
 L’atrophie progressive de la rétine (PRA en anglais) désigne un groupe de maladies génétiques affectant la rétine et impliquant la dégénérescence progressive des cellules réceptrices de la lumière en bâtonnet et en cône.
L’atrophie progressive de la rétine (PRA en anglais) désigne un groupe de maladies génétiques affectant la rétine et impliquant la dégénérescence progressive des cellules réceptrices de la lumière en bâtonnet et en cône.
Les cellules réceptrices en bâtonnet détectent la lumière faible et sont utiles pour la vision nocturne ainsi que pour la vision périphérique. Les cellules réceptrices en cône détectent la vision des couleurs et sont utiles pour la vision diurne. La PRA de type 1 de l’épagneul nain continental est une maladie génétique de la rétine pour laquelle les signes cliniques apparaissent pour la première fois vers l’âge de 4 à 6 ans.
Les signes cliniques de la PRA de Type 1
Puisque que les cellules réceptrices en bâtonnets sont les premières à être affectées, les chiens double mutés commenceront par perdre leur vision nocturne et périphérique. Le développement de la maladie est lent, mais progressif ; les cellules réceptrices en cônes sont éventuellement atteintes et les chiens commencent à perdre leur vision du jour. Un chien atteint peut conserver une vision limitée pendant plusieurs années, mais la maladie aboutit généralement à la cécité.
PRA de Type 1, une nouvelle mutation
 L’épagneul nain continental / Papillon est un petit épagneul décrit par l’American Kennel Club comme amical, alerte et heureux. Bien que les épagneuls nains continentaux soient une race ancienne, la PRA de Type 1 les affectant est une maladie nouvellement reconnue, décrite pour la première fois dans la littérature scientifique en 1995.
L’épagneul nain continental / Papillon est un petit épagneul décrit par l’American Kennel Club comme amical, alerte et heureux. Bien que les épagneuls nains continentaux soient une race ancienne, la PRA de Type 1 les affectant est une maladie nouvellement reconnue, décrite pour la première fois dans la littérature scientifique en 1995.
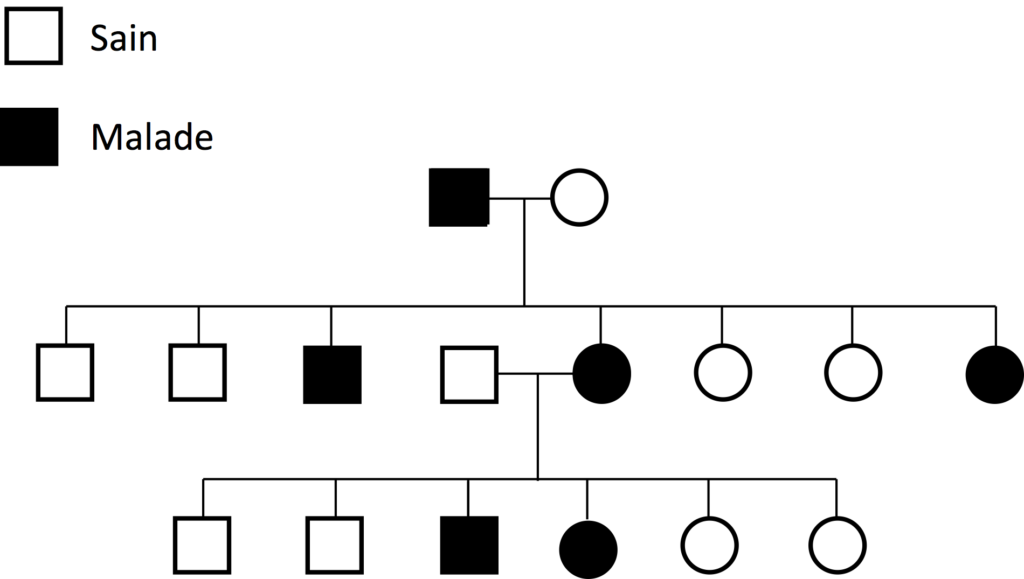
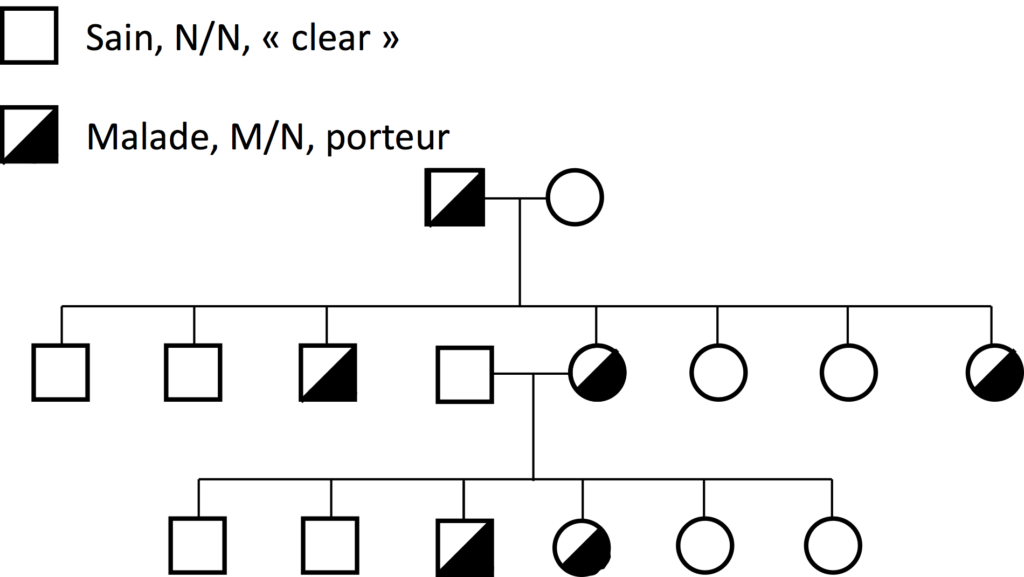
C’est un exemple d’une maladie génétique qui n’a été observée que chez une seule race. Génétiquement, le PRA de Type 1 se comporte comme une maladie génétique autosomique récessive typique, où les chiens atteints de la maladie sont double muté M/M et les chiens non malades sont « clear » N/N ou porteurs M/N.
Clubs de race Papillon proactifs
 La PRA-Type-1 est causée par une mutation assez compliquée du gène CNGB1 qui combine une délétion et une insertion qui a été décrite en 2013. Les clubs de la race épagneul nain continental en Amérique du Nord sont particulièrement actifs pour tenter d’éliminer la mutation de leurs animaux reproducteurs.
La PRA-Type-1 est causée par une mutation assez compliquée du gène CNGB1 qui combine une délétion et une insertion qui a été décrite en 2013. Les clubs de la race épagneul nain continental en Amérique du Nord sont particulièrement actifs pour tenter d’éliminer la mutation de leurs animaux reproducteurs.
Chez Labgenvet, nous effectuons nos tests par séquençage d’ADN, ce qui permet d’identifier facilement les animaux N/N, M/N et M/M. Depuis 2016, nous avons testé plus de 80 échantillons envoyés par les éleveurs d’Épagneuls nains continentaux pour cette maladie.
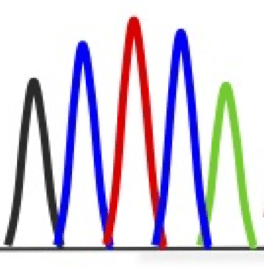
Les profils et les fréquences de séquençage d’ADN
Voici des profils de séquençage d’ADN représentatifs et les fréquences de mutation que nous avons pu voir à Labgenvet :
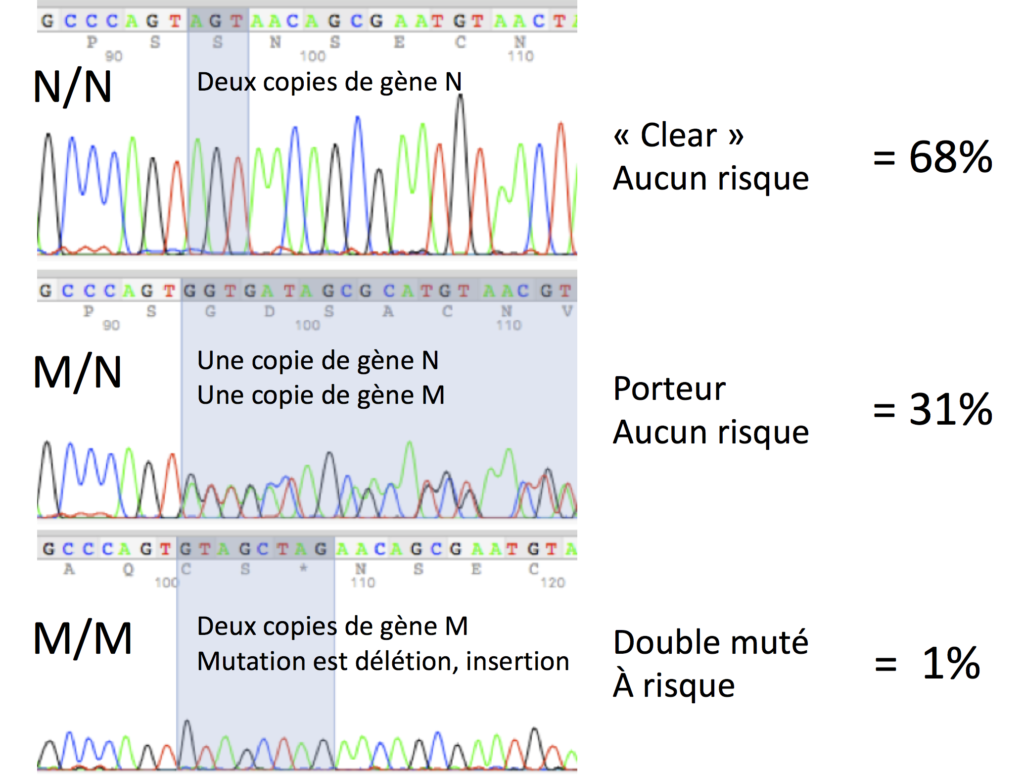
Bien que la probabilité d’avoir un animal double muté M/M à risque de dégénérescence rétinienne soit faible, la probabilité d’avoir un animal porteur M/N est en fait assez élevée. Ces probabilités seront réduites avec le temps, car les éleveurs d’Épagneuls nains continentaux / Papillons continuent d’utiliser le test ADN pour les aider dans leurs décisions d’accouplement.
Hypersensibilité aux médicaments (MDR1)
 L’hypersensibilité aux médicaments (ou MDR1) est une maladie génétique dans laquelle les chiens porteurs de mutations dans le gène ABCB1 (également appelé gène MDR1) sont hypersensibles aux médicaments vétérinaires couramment utilisés. Pour cette raison, la MDR1 est considérée comme une maladie génétique pharmacologique.
L’hypersensibilité aux médicaments (ou MDR1) est une maladie génétique dans laquelle les chiens porteurs de mutations dans le gène ABCB1 (également appelé gène MDR1) sont hypersensibles aux médicaments vétérinaires couramment utilisés. Pour cette raison, la MDR1 est considérée comme une maladie génétique pharmacologique.
Le gène la MDR1 code pour une protéine de transport qui protège le cerveau des petites molécules toxiques en les fixant et en les transportant hors du cerveau. Un chien avec deux copies mutées du gène MDR1 est particulièrement sensible à la toxicité de toute une gamme de médicaments couramment utilisés en médecine vétérinaire, notamment les médicaments antiparasitaires (lactones macrocycliques comme l’ivermectine), les antibiotiques (comme l’érythromycine), les médicaments antidiarrhéiques (tels que le lopéramide), les tranquillisants (tels que l’acépromazine), les opioïdes (tels que le butorphanol) et d’autres médicaments, y compris les agents chimiothérapeutiques anticancéreux (tels que la vincristine, la vinblastine, la doxorubicine).
Les signes cliniques de la MDR1
Les signes de toxicité peuvent inclure une perte de vigilance, une salivation excessive, une dilatation des pupilles, des tremblements, une ataxie, des convulsions, un ralentissement du rythme cardiaque, un coma, un arrêt respiratoire et la mort. Notez que les signes de toxicité sont beaucoup plus sévères chez l’animal double muté, mais sont parfois signalés chez des animaux porteurs d’une seule mutation. C’est pour cela que l’hérédité de l’hypersensibilité aux médicaments est considérée comme dominante avec une pénétrance variable. Alors, bien que l’animal double muté (M/M) soit le plus à risque de présenter une toxicité sévère pour les médicaments, il convient toutefois de faire preuve de prudence lors de l’administration de médicaments à des animaux porteurs (M/N).
MDR1 et les races bergers
 La mutation de la MDR1 se retrouve chez un certain nombre de races de chiens, principalement de type berger et colley ou de leurs croisements. Ces races comprennent : Berger allemand, Berger américain miniature, Berger anglais, Berger australien, Berger australien miniature, Berger blanc suisse, Berger des Shetland, Berger McNab, Berger Picard, Border Collie, Bouvier australien, Chinook, Colley, Colley à poil court, Collie à poil long, Koolie, Lévrier de soie, Lévrier whippet à poil long, Old English Sheepdog (Bobtail), Ryukyu Inu, Shiloh Shepherd, Waller.
La mutation de la MDR1 se retrouve chez un certain nombre de races de chiens, principalement de type berger et colley ou de leurs croisements. Ces races comprennent : Berger allemand, Berger américain miniature, Berger anglais, Berger australien, Berger australien miniature, Berger blanc suisse, Berger des Shetland, Berger McNab, Berger Picard, Border Collie, Bouvier australien, Chinook, Colley, Colley à poil court, Collie à poil long, Koolie, Lévrier de soie, Lévrier whippet à poil long, Old English Sheepdog (Bobtail), Ryukyu Inu, Shiloh Shepherd, Waller.
Cette liste de races indique que la mutation à l’origine du problème est assez ancienne et qu’elle s’est produite avant la ségrégation des races de type berger de leur forme actuelle.
L’intolérance des médicaments
 La mutation à l’origine de la MDR1 est une délétion de quatre bases dans le gène ABCB1. Pour qu’une intoxication se produise, les chiens doivent recevoir un produit pharmacologique. Les chiens qui sont « clear » (N/N) pour la mutation auront une tolérance normale aux médicaments. Les chiens qui ont une copie normale et une copie mutée de la mutation (M/N) semblent avoir une tolérance quelque peu réduite (c’est-à-dire une toxicité accrue) aux médicaments.
La mutation à l’origine de la MDR1 est une délétion de quatre bases dans le gène ABCB1. Pour qu’une intoxication se produise, les chiens doivent recevoir un produit pharmacologique. Les chiens qui sont « clear » (N/N) pour la mutation auront une tolérance normale aux médicaments. Les chiens qui ont une copie normale et une copie mutée de la mutation (M/N) semblent avoir une tolérance quelque peu réduite (c’est-à-dire une toxicité accrue) aux médicaments.
Le véritable problème clinique et l’animal à qui il faut éviter de donner des médicaments est l’animal double muté (M/M), pour lequel des doses de médicaments normalement sans danger deviennent hautement toxiques. La mutation a été signalée en 2001. Les éleveurs et les vétérinaires ont donc eu accès à des tests d’ADN pour identifier les porteurs et les animaux à risque, depuis près de vingt ans maintenant. Malgré cela, nous observons toujours des animaux M/N et M/M.
Les profils et les fréquences de séquençage d’ADN
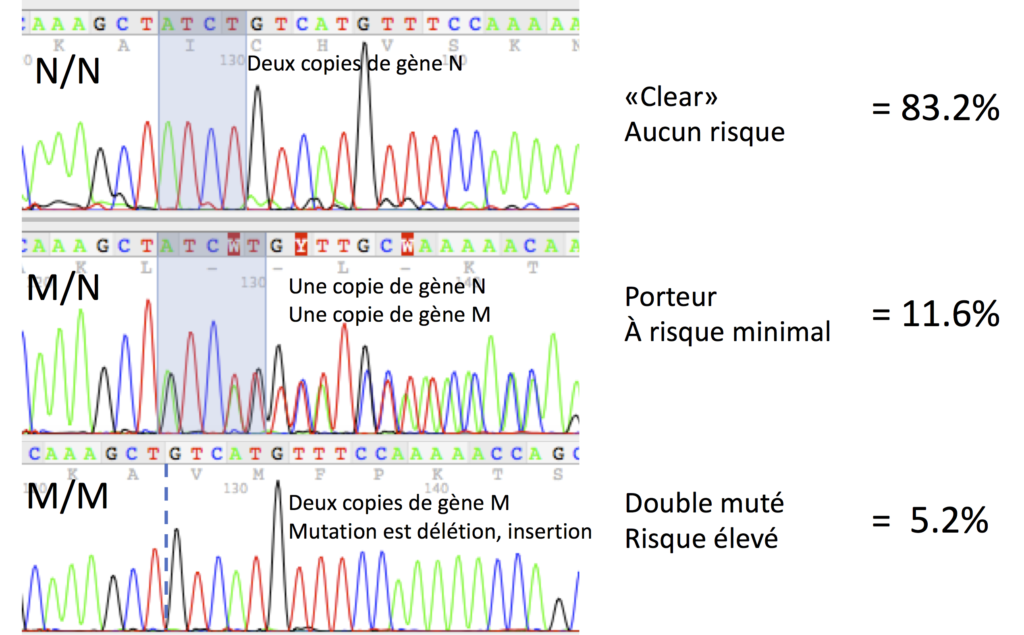
Les statistiques et les profils de séquençages suivants ont été rassemblés sur plus de 400 échantillons à Labgenvet :
Myélopathie dégénérative (DM)

Berger allemand
La myélopathie dégénérative (DM) est une maladie dégénérative neuromusculaire causée par une mutation génétique identifiée chez de nombreuses races de chien. Les facteurs environnementaux ainsi que d’autres facteurs génétiques peuvent contribuer à l’apparition et à la progression de la maladie. La DM est une maladie qui affecte la substance blanche de la moelle épinière et elle est équivalente à la sclérose latérale amyotrophique (SLA), également connue sous le nom de maladie de Lou Gehrig chez l’Homme.
Les signes cliniques de la myélopathie dégénérative
Les chiens atteints commencent généralement à présenter des symptômes d’atrophie musculaire progressive vers l’âge de 7 à 9 ans, avec une perte initiale de coordination des membres postérieurs. Ces chiens peuvent perdre leur mobilité six mois à deux ans après l’apparition des premiers signes cliniques, les gros chiens présentant une progression des symptômes plus rapide que les petits chiens.
La douleur n’est pas associée à la maladie et les symptômes peuvent évoluer au point que l’animal est incontinent et éventuellement paraplégique. Malheureusement, n’y a pas de traitements qui existent. Souvent, l’animal affecté est euthanasié pour des raisons humanitaires avant d’arriver à ces derniers stades.
La génétique de la myélopathie dégénérative

Bouvier bernois
La DM chez les chiens est un exemple de maladie génétique qui suit (plus ou moins) une génétique simple ou mendélienne. La mutation de l’ADN liée à la DM est une simple substitution d’une lettre par une autre trouvée dans le gène SOD1. Cette mutation a été identifiée chez plus de 180 races de chiens, dont je ne pourrais pas toutes vous les énumérer.
La DM est considérée comme une maladie autosomique récessive à la pénétrance variable. Des chiens de plusieurs races sont particulièrement à risque de développer la DM lorsqu’ils sont double mutés (M/M). Parmi ces races figurent, entre autres, le Berger allemand, le Bouvier bernois et le Boxer.
Les gènes modificateurs de la myélopathie dégénérative

Corgi
Pour certaines races de chien, les chiens peuvent être M/M pour la mutation du gène SOD1, mais peuvent développer ou non la myélopathie dégénérative, selon des facteurs génétiques supplémentaires appelés gènes modificateurs.
Un exemple est le Welsh Corgi Pembrooke. Les Corgis M/M pour la mutation du gène SOD1 peuvent présenter des signes cliniques de DM à l’âge de 7 à 9 ans ou peuvent être exempts de signes à l’âge de 15 ans. La susceptibilité accrue semble être due à la présence d’une mutation dans un gène modificateur qui a été identifié chez les Corgis. Malheureusement, les gènes modificateurs d’autres races, même s’ils ne sont encore que suspectés, ne sont pas encore identifiés.
Le Bouvier bernois est une autre race qui mérite d’être mentionnée. En effet, une seconde mutation dans le gène pouvant entraîner une augmentation de risques et de symptômes de la DM a été identifiée chez cette race. Cette seconde mutation n’est pas observée chez les autres races. Ainsi, on peut constater que la génétique simple n’est donc pas toujours simple. La génétique connue de la DM chez le chien demeure toutefois moins complexe par rapport à la génétique connue de la SLA chez l’Homme, où il existe plus de 150 mutations documentées dans le gène SOD1 humain et au moins 5 gènes modificateurs différents qui ont été identifiés pour la SLA.
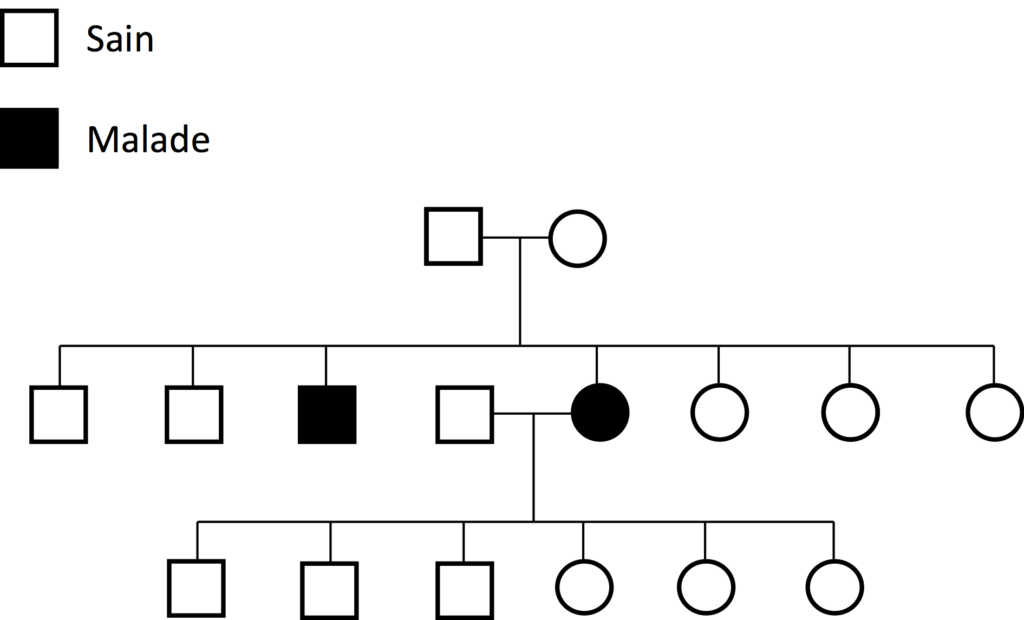
Une maladie récessive survenant plus tard dans la vie
Il y a plusieurs aspects pratiques concernant la DM chez les chiens qui méritent d’être mentionnés. C’est une maladie récessive qui survient plus tard dans la vie, après les années de reproduction de l’animal. Bien entendu, les animaux doubles mutés M/M présentant des symptômes posent un problème, mais les animaux porteurs non identifiés (M/N) constituent un problème supplémentaire, en particulier en ce qui concerne la lutte contre la maladie chez une race.
Si les animaux M/N sont inconsciemment utilisés pour la reproduction, il y a de fortes chances que la mutation soit transmise à la génération suivante. Plus problématique encore, si deux animaux M/N sont reproduits ensemble, il y a une chance sur quatre de produire des chiots double mutés M/M qui sont à risque de développer la maladie plus tard dans la vie et ainsi le cycle de la maladie se poursuit. Ces chiots existent parce que je vois leur ADN alors, je sais qu’à 7 ou 9 ans, ils seront emmenés dans une clinique vétérinaire parce qu’ils commencent à avoir la perte de coordination des membres postérieurs.
Identifier les animaux porteurs

Boxer
Bien que les animaux porteurs non identifiés soient un problème, dès que ceux-ci sont identifiés (généralement par un test ADN), ils deviennent beaucoup moins problématiques. Les animaux porteurs ne courent aucun risque de développer la maladie et s’ils sont reproduits avec des animaux « clear » N/N, il n’y a aucun risque de produire des chiots doublement mutés M/M. Comme je tiens souvent à dire aux éleveurs, l’identification d’un animal porteur (M/N) est une bonne nouvelle, même s’ils auraient bien évidemment préféré identifier un animal « clear » (N/N). C’est l’identification de l’animal porteur qui est important.
Quoi qu’il en soit, en raison du nombre de races de chiens porteurs de la mutation SOD1, la fréquence de la mutation observée au sein des races, de l’âge tardif de la maladie, de la génétique « simple » plutôt compliquée ainsi que de la nature décentralisée de l’élevage de chiens, il faudra de nombreuses années avant que la DM et sa mutation soient éliminées de nos races de chiens.
Les profils et les fréquences de séquençage d’ADN
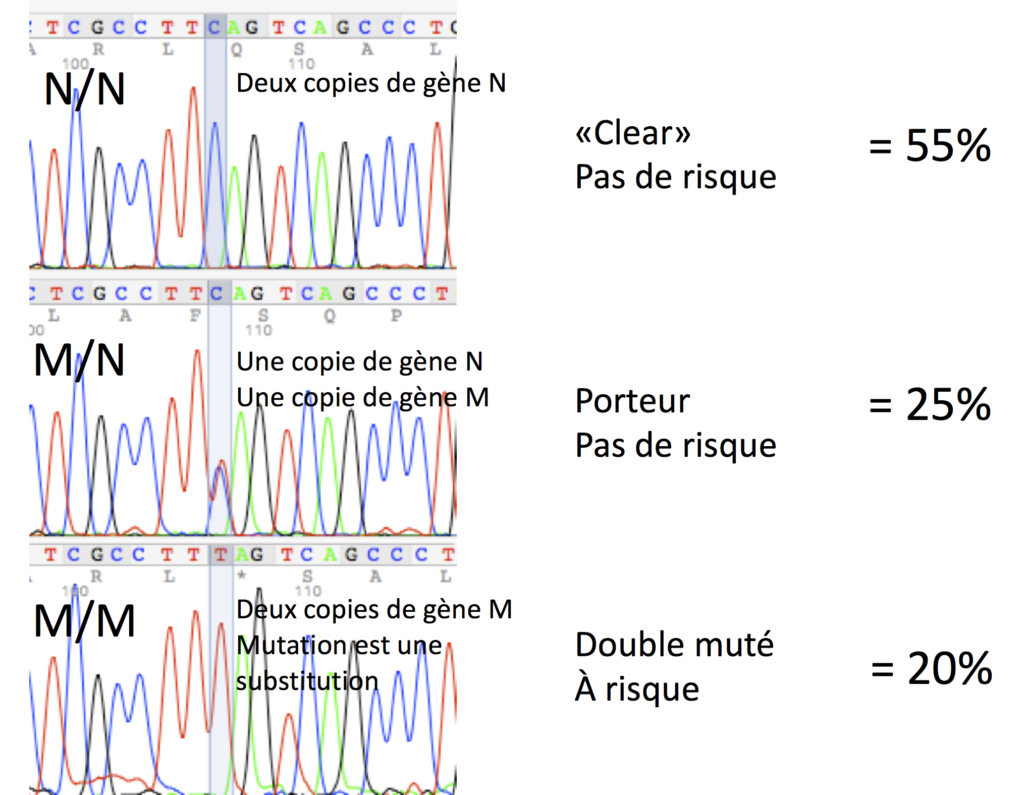
Les profils de séquençage de l’ADN et les fréquences des animaux N/N « clear », M/N (porteurs) et M/M (double mutés) pour la mutation de la DM, sur une base de plus de 600 chiens testés à Labgenvet, sont les suivants :
La connaissance est un pouvoir et le pouvoir est une responsabilité

Nos connaissances sur la base mutationnelle des maladies génétiques simples chez le chien augmentent chaque année. Avec les bons tests d’ADN validés, nous avons maintenant le pouvoir d’identifier les animaux porteurs (M/N).
Nous pourrions en théorie éliminer une maladie génétique simple d’une race donnée au sein d’une génération d’élevage et éliminer la mutation causant la maladie en deux générations. Le défi consiste à assumer cette responsabilité.
Les maladies génétiques ne sont pas toujours aussi simples

Ce que j’ai présenté jusqu’ici est valable pour la génétique simple ou mendélienne, où un seul gène muté cause la maladie. Cependant, il existe plus de 20 000 gènes codant pour des protéines dans le génome du chien et les gènes ne fonctionnent pas de manière isolé. Les maladies génétiques complexes, impliquant la contribution de mutations dans plusieurs gènes ainsi que des apports environnementaux, ne suivent pas les règles génétiques simples dont nous venons de parler.
La dysplasie de la hanche chez le chien est un exemple de maladie génétique complexe avec de multiples apports génétiques (encore indéterminés) et une forte implication environnementale. Les problèmes de santé associés à des conformations exagérées (visage court, pattes courtes, queue courte, dos long, oreilles tombantes, etc.) sont en fait des maladies génétiques qui se retrouvent dans le grand désordre de conformation des races. La vie et la génétique ne sont pas toujours simples, même si nous souhaitons qu’elles le soient.
© 2020 Dr David W. Silversides
 La prévalence des maladies génétiques chez nos chiens est un problème connu et de longue date dont la difficulté est double. Tout d’abord, d’un côté, nous avons des chiens qui sont malades à cause d’une maladie génétique et d’un autre côté, nous avons des chiens en parfaite santé, mais qui sont porteurs d’une mutation causant une maladie.
La prévalence des maladies génétiques chez nos chiens est un problème connu et de longue date dont la difficulté est double. Tout d’abord, d’un côté, nous avons des chiens qui sont malades à cause d’une maladie génétique et d’un autre côté, nous avons des chiens en parfaite santé, mais qui sont porteurs d’une mutation causant une maladie. Les mutations anciennes et les mutations anciennes recentes
Les mutations anciennes et les mutations anciennes recentes