Profil de maladie canine – Myélopathie dégénérative (DM)
Rédaction par Dr David W. Silversides, DVM
La myélopathie dégénérative (DM) est une maladie dégénérative neuromusculaire causée par une mutation génétique identifiée chez de nombreuses races de chien. Les facteurs environnementaux ainsi que d’autres facteurs génétiques peuvent contribuer à l’apparition et à la progression de la maladie. La DM est une maladie qui affecte la substance blanche de la moelle épinière et elle est équivalente à la sclérose latérale amyotrophique (SLA), également connue sous le nom de maladie de Lou Gehrig chez l’Homme.
Signes cliniques de la myélopathie dégénérative
Les chiens atteints commencent généralement à présenter des symptômes d’atrophie musculaire progressive vers l’âge de 7 à 9 ans, avec une perte initiale de coordination des membres postérieurs. Ces chiens peuvent perdre leur mobilité six mois à deux ans après l’apparition des premiers signes cliniques, les gros chiens présentant une progression des symptômes plus rapide que les petits chiens.
La douleur n’est pas associée à la maladie et les symptômes peuvent évoluer au point que l’animal est incontinent et éventuellement paraplégique. Malheureusement, n’y a pas de traitements qui existent. Souvent, l’animal affecté est euthanasié pour des raisons humanitaires avant d’arriver à ces derniers stades.
La génétique de la myélopathie dégénérative
La DM chez les chiens est un exemple de maladie génétique qui suit (plus ou moins) une génétique simple ou mendélienne. La mutation de l’ADN liée à la DM est une simple substitution d’une lettre par une autre trouvée dans le gène SOD1. Cette mutation a été identifiée chez plus de 180 races de chiens, dont je ne pourrais pas toutes vous les énumérer.
La DM est considérée comme une maladie autosomique récessive à pénétrance variable. Des chiens de plusieurs races sont particulièrement à risque de développer la DM lorsqu’ils sont double mutés (M/M). Parmi ces races figurent, entre autres, le Berger allemand, le Bouvier bernois et le Boxer.
Les gènes modificateurs de la myélopathie dégénérative
Pour certaines races de chien, les chiens peuvent être M/M pour la mutation du gène SOD1, mais peuvent développer ou non la myélopathie dégénérative, selon des facteurs génétiques supplémentaires appelés gènes modificateurs.
Un exemple est le Welsh Corgi Pembrooke. Les Corgis M/M pour la mutation du gène SOD1 peuvent présenter des signes cliniques de DM à l’âge de 7 à 9 ans ou peuvent être exempts de signes à l’âge de 15 ans. La susceptibilité accrue semble être due à la présence d’une mutation dans un gène modificateur qui a été identifié chez les Corgis. Malheureusement, les gènes modificateurs d’autres races, même s’ils ne sont encore que suspectés, ne sont pas encore identifiés.
Le Bouvier bernois est une autre race qui mérite d’être mentionnée. En effet, une seconde mutation dans le gène pouvant entraîner une augmentation de risques et de symptômes de la DM a été identifiée chez cette race. Cette seconde mutation n’est pas observée chez les autres races. Ainsi, on peut constater que la génétique simple n’est donc pas toujours simple. La génétique connue de la DM chez le chien demeure toutefois moins complexe par rapport à la génétique connue de la SLA chez l’Homme, où il existe plus de 150 mutations documentées dans le gène SOD1 humain et au moins 5 gènes modificateurs différents qui ont été identifiés pour la SLA.
Une maladie récessive survenant plus tard dans la vie
Il y a plusieurs aspects pratiques concernant la DM chez les chiens qui méritent d’être mentionnés. C’est une maladie récessive qui survient plus tard dans la vie, après les années de reproduction de l’animal. Bien entendu, les animaux doubles mutés M/M présentant des symptômes posent un problème, mais les animaux porteurs non identifiés (M/N) constituent un problème supplémentaire, en particulier en ce qui concerne la lutte contre la maladie chez une race.
Si les animaux M/N sont inconsciemment utilisés pour la reproduction, il y a de fortes chances que la mutation soit transmise à la génération suivante. Plus problématique encore, si deux animaux M/N sont reproduits ensemble, il y a une chance sur quatre de produire des chiots double mutés M/M qui sont à risque de développer la maladie plus tard dans la vie et ainsi le cycle de la maladie se poursuit. Ces chiots existent parce que je vois leur ADN alors, je sais qu’à 7 ou 9 ans, ils seront emmenés dans une clinique vétérinaire parce qu’ils commencent à avoir la perte de coordination des membres postérieurs.
Identifier les animaux porteurs
Bien que les animaux porteurs non identifiés soient un problème, dès que ceux-ci sont identifiés (généralement par un test ADN), ils deviennent beaucoup moins problématiques. Les animaux porteurs ne courent aucun risque de développer la maladie et s’ils sont reproduits avec des animaux « clear » N/N, il n’y a aucun risque de produire des chiots doublement mutés M/M. Comme je tiens souvent à dire aux éleveurs, l’identification d’un animal porteur (M/N) est une bonne nouvelle, même s’ils auraient bien évidemment préféré identifier un animal « clear » (N/N). C’est l’identification de l’animal porteur qui est important.
Quoi qu’il en soit, en raison du nombre de races de chiens porteurs de la mutation SOD1, la fréquence de la mutation observée au sein des races, de l’âge tardif de la maladie, de la génétique « simple » plutôt compliquée ainsi que de la nature décentralisée de l’élevage de chiens, il faudra de nombreuses années avant que la DM et sa mutation soient éliminées de nos races de chiens.
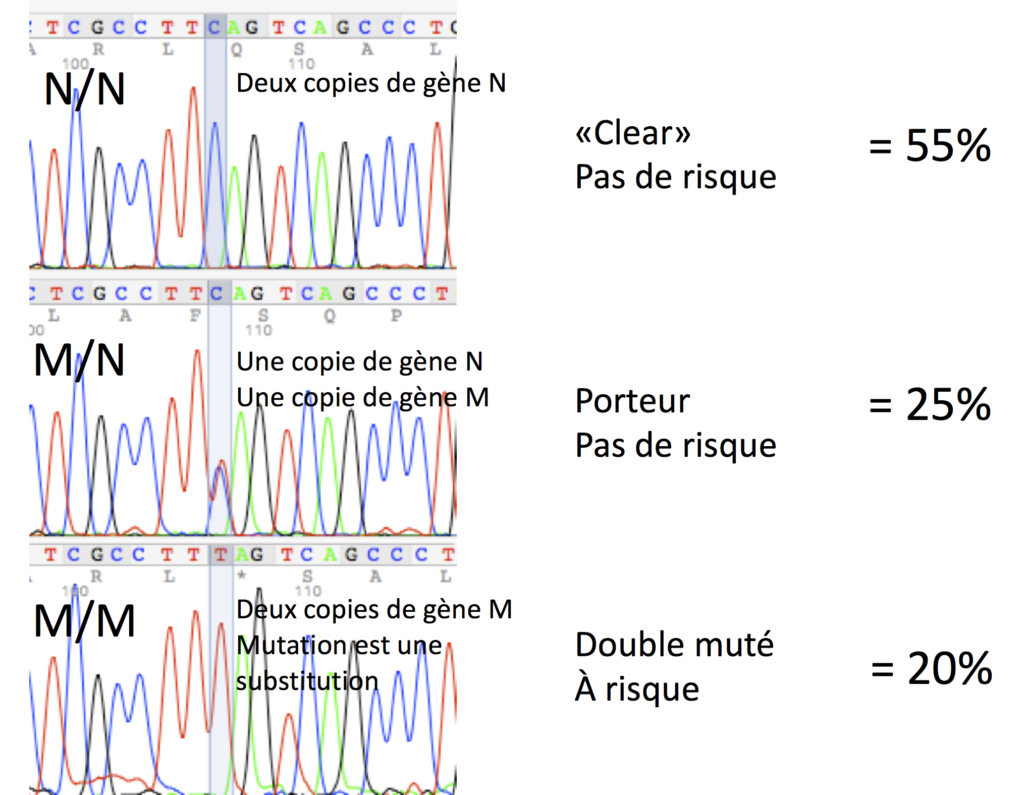
Les profils et les fréquences de séquençage d’ADN
Les profils de séquençage de l’ADN et les fréquences des animaux N/N « clear », M/N (porteurs) et M/M (double mutés) pour la mutation de la DM, sur une base de plus de 600 chiens testés à Labgenvet, sont les suivants :
Pour obtenir des informations génétiques supplémentaires et des références concernant la myélopathie dégénérative (DM) chez le chien, veuillez consulter le lien suivant: https://labgenvet.ca/maladie/myelopathie-degenerative-dm-sod1/.
Une liste complète des maladies génétiques simples chez les chiens est disponible à l’adresse suivante: https://labgenvet.ca/recherche-de-maladies-genetiques-canines/.
References:
- OMIA link [000263-9615]
- Awano T, Johnson GS, Wade CM, Katz ML et al. (2009) Genome-wide association analysis reveals a SOD1 mutation in canine degenerative myelopathy that resembles amyotrophic lateral sclerosis. PNAS 106(8), 2794-2799. [pubmed/19188595]
- Zeng R, Coates JR, Johnson GC et al. (2014) Breed distribution of SOD1 alleles previously associated with canine degenerative myelopathy. J Vet Intern Med 28(2):515-521. [pubmed/24524809]
- Coates JR, Wininger FA. (2010) Canine degenerative myelopathy. Vet Clin North Am Small Anim Pract. 40(5):929-50. [pubmed/20732599]
- Crisp MJ, Beckett J, Coates JR, Miller TM. (2013) Canine degenerative myelopathy: biochemical characterization of superoxide dismutase 1 in the first naturally occurring non-human amyotrophic lateral sclerosis model. Exp Neurol. 248:1-9. [pubmed/23707216]
- Holder AL, Price JA, Adams JP, Volk HA, Catchpole B. (2014) A retrospective study of the prevalence of the canine degenerative myelopathy associated superoxide dismutase 1 mutation (SOD1:c.118G > A) in a referral population of German Shepherd dogs from the UK. Canine Genet Epidemiol. 1:10. [pubmed/26401327]
- Turba ME, Loechel R, Rombola E et al. (2017) Evidence of a genomic insertion in intron 2 of SOD1 causing allelic drop-out during routine diagnostic testing for canine degenerative myelopathy. Animal Genetics 48(3):365-368. [pubmed/27917507]